Dr. Thomas Habot, Aarhus University Hospital, Danemark
- ANX005 est un anticorps monoclonal innovant administré par voie orale induisant l’inhibition de C1q et, en conséquence, de toutes la voie classique du complément, permettant de réduire les lésions tissulaires dans le syndrome de Guillain-Barré.
- ANX005 a déjà été testé dans un essai de phase 1b contrôlé contre placebo. La tolérance est bonne avec les différentes doses de ce traitement.
Dans cet abstract, l’auteur présente les résultats d’un essai ouvert visant a démontrer l’efficacité d’une thérapie combinée : ANX005 et de IvIG dans le cadre du traitement des formes sévères de SGB.
Population étudiée
- 11 patients suivis au Bangladesh et 3 patients suivis en Danemark ont été inclus dans l’essai pour un total de 14 patients (80% d’hommes).
- Tous les patients ont été traités entre 7 et 9 jours après le début des symptômes liés au SGB.
- Le GBS score a l’inclusion était > ou = 3
- Chaque patient a été traité par une dose unique de ANX005 75 mg/kg, administré en add-on du traitement standard par IgIV.
- Les patients ont été suivis pendant 26 semaines.
- Le testing manuel de la force musculaire aux quatre membres a été utilisé comme critère de jugement principal (valeur moyenne a l’inclusion = 20.1)
- Un dosage de la chaine légère des Neurofilaments sériques a été utilisé comme critère secondaire.
Résultats préliminaires
1) Sécurité et tolérance du médicament
- Tous les 14 patients traités ont présenté au moins 1 évènement indésirable non sévère
- réactions cutanées suite à la perfusion de dégrée modérée, douleur au site d’injection
- Un seul patient a présenté un évènement indésirable grave (fièvre, EP) considéré comme non lié au traitement.
- Toutes les réactions liées aux perfusions du produit ANX005 ont été transitoires. Aucune infection n’a été relevée.
2) Pharmacocinétique et pharmacodynamique
- Une interaction directe entre l’ ANX005 et le facteur C1q du complément a été démontré chez les patients traités.
- L’inhibition de l’activité du complément a été maintenue pendant 3 semaines.
Résultats
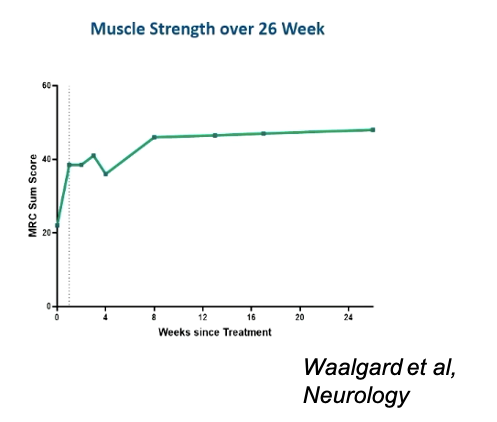
- Une amélioration de la force musculaire aux quatre membres a été démontrée dès la première semaine après le début du traitement.
- L’amélioration du score MRC semble être plus précoce par rapport à l’amélioration fonctionnelle mesurée par le GBS score.
- Deux groupes différents de sujets one été identifiés à la baseline sur la base du score MRC et du taux sérique de NFL avec des différentes trajectoires d’amélioration au cours du temps.
- Les patients qui présentaient une atteinte neuromusculaire moins sévère au début de la maladie ont eu une amélioration plus rapide des symptômes par rapport aux patients les plus sévères.
- Le taux sérique de NfL était élévé chez tous les sujets.
- Le taux sérique de NfL est résulté être directement corrélé avec l’outcome des patients après 26 semaines d’observation (r de Spearmann = 0.86).
- Une réduction progressive du taux sérique de NfL a été observée après le traitement = bon biomarqueur pronostique
Résumé
- La combinaison de IgIV et ANX005 est bien toléré chez les patients atteints de SGB.
- L’ ANX005 est capable de se lier de façon efficace au fragment C1q du complément
- La suppression de l’activité de C1q est maintenue pour 1-3 semaines.
- Le taux sérique de NFL et la MRC à la baseline sont prédicteurs de la vitesse d’amélioration après le traitement (les patients avec un MRC plus élévé et un taux de NFL plus faible s’améliorant plus rapidement).
- Une étude de phase 2/3 contrôlé contre placebo sera mise en place pour tester l’efficacité de ANX005 en monothérapie dans les formes modérées à sévères du syndrome de Guillain Barré.
 Espace adhérent
Espace adhérent